三、诊断题(本大题1小题,15分)
23.某化学教师在一次化学测验中设计了下列试题,并对部分学生的解题结果进行了统计和分析。
【试题】某同学设计了一个实验方案,用以检验淀粉的水解情况。
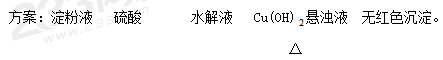
结论:淀粉完全没有水解。
讨论上述方案的设计及结论是否正确?请简述理由。
【考试结果】有32.6%的学生提交的错误答案是:设计的方案和结论均正确。因为没有红色沉淀生成,证明溶液中没有水解产物葡萄糖,所以淀粉完全没有水解。
根据上述信息,回答下列问题:
(1)你认为正确的答案是:________。(6分)
(2)对学生解题错误形成的原因进行分析和诊断。(5分)
(3)请设计一个实验方案,证明淀粉是否完全水解。(4分)
四、案例分析题(本大题l小题,20分)阅读案例,并回答问题。
24.案例:
某版本化学教科书“金属钠的性质与应用”的片断
1.观察下列实验,并将观察到的现象及所得的结论填入表2—3. 【实验1】取一小块金属钠,用滤纸吸干表面的煤油,用小刀切去一端的表层,观察表面的颜色;将其放置在空气中,观察表面颜色的变化。 【实验2】将一小块金属钠放在石棉网上加热,观察现象。 【实验3】向一只盛有水的小烧杯中滴加几滴酚酞溶液,然后投入一小块(约绿豆粒大小)金属钠,观察实验现象。 表2-3钠的性质实验 实验现象 结论(或化学方程式) 实验1 实验2 实验3 2.根据上述反应中钠元素化合价的变化情况,总结钠在反应中体现出的性质。 |
问题:
(1)“金属钠的性质与应用”属于普通高中______________模块的内容(填模块名称)。(2分)
(2)实验1、2、3中观察到的实验现象是:
实验1_________________________________________________________;(2分)
实验2_________________________________________________________;(2分)
实验3__________________________________________________________。(2分)
(3)根据实验l、2、3中观察到的实验现象总结钠在反应中体现出的性质。(4分)
(4)在[实验2]中,观察到少量黑色物质的出现,试分析产生这种现象的可能原因。(4分)
(5)在中学化学实验教学中,应该如何指导学生进行实验观察?(4分)
五、教学设计题(本大题1小题,30分)
25.阅读下列三个有关材料。
材料一化学课程标准的内容标准
根据生产、生活中的应用实例或通过实验探究,了解钠、铝、铁、铜等金属及其重要化合物的主要性质,能列举合金材料的重要作用。
材料二教科书的知识结构体系
第1章认识化学科学
第2章元素与物质世界
第3章 自然界中的元素
第4章材料家族中的元素
第1节硅无机非金属材料
第2节铝金属材料
第3节复合材料
材料三教科书“铝与铝合金”的呈现内容
1. 认识铝及其化合物 【交流、研讨】 你已经学习过钠、镁、铁等金属单质的知识,这些金属在性质上具有相似之处。 讨论:1.铝作为一种金属,它可能具有哪些性质? 2.铝是一种重要的金属材料,这可能与它具有的哪些性质有关? 铝(aluminum)是一种银白色金属,熔点为660.4℃,沸点为2467℃;密度为2.7g/cm3仅为钢的1/3左右;导电性仅次于银、铜和金。 金属铝的化学性质活泼,它容易与氧气发生反应。常温下,金属铝被空气里的氧气氧化,在表面生成一层致密的氧化物薄膜,这层薄膜能阻止内部的金属继续与氧气发生反应。铝还能与金属氧化物发生反应,表现出较强的还原性。 【观察·思考】 金属铝的还原性 【实验1】用镊子夹住一小团脱脂棉,蘸上一些铝粉,在酒精灯上点燃,并立即伸入盛有氧气的集气瓶中(瓶底放一些细沙),观察发生的现象。 【实验2】将两张圆形滤纸分别折叠成漏斗状并套在一起,使四周都是四层。把内层 “纸漏斗”取出,在底部剪一个孔,用水湿润,再与另一“纸漏斗”套在一起,架在铁架台的铁圈上,下面放置盛有细沙的蒸发皿。把59炒干的三氧化二铁粉末和29铝粉混合均匀,放在“纸漏斗”中,上面加少量氯酸钾并在混合物中插一根镁条,用然着的木条点燃镁条,观察发生的现象。
四羟基合铝酸钠 |
(摘自某版本普通高中课程标准实验教科书《4匕学1》第4章、第2节“铝金属材料”)
根据上述材料,回答下列有关问题:
(1)确定本课的三维教学目标。(6分)
(2)确定本课的教学重点和难点。(4分)
(3)用教学流程图(教学设计思路)-简要表示本节教学内容组织形式。(6分)
(4)在[实验2]铝热反应实验中,简述“纸漏斗”上面加入少量氯酸钾的原因.并写出相关化学反应方程式。(5分)
(5)回答【交流·研讨】中问题2:“铝是一种重要的金属材料,这可能与它具有的哪些性质有关”。(3分)
(6)对本课教学内容进行板书设计。(6分)
24.【参考解析】
(1)化学必修 1
(2)实验 1:钠表面由光亮的银白色逐渐暗淡。
实验2:钠首先熔化成球状,然后剧烈燃烧,发出黄色光,生成淡黄色粉固体。
实验3:钠浮于水面上;和水发生剧烈的反应,反应中放出的热量能使金属钠熔化成小
球;产生的气体使钠四处游动,发出嘶嘶的响声;生成碱性物质,因而溶液变红。
(3)由钠容易切割体现了钠的硬度低;保存在煤油中、钠表面由光亮的银白色逐渐暗淡、加热剧烈燃烧表明钠容易被空气氧化;与水可以发生剧烈的化学反应生成氢气和氢氧化钠体现了强的还原性;加热和与水反应放出的热量使钠熔化成球状体现了熔点低。
(4) 钠 与 空 气 中 的 二 氧 化 碳 反 应 , 产 生 还 原 产 生 C, 化 学 反 应 方 程 式 为 :
4Na+3CO2=C+2Na2CO3
(5)①明确实验目的和实验观察的重点;
②调动学生多种感官进行全面观察;
③引导学生集中精力,及时记录实验信息;
④引导学生客观观察,如实记录现象。
五、教学设计题(本大题1 小题,30 分)
25.【参考解析】
(1)三维教学目标:
知识目标:
①理解铝及其氧化物的性质。
②掌握铝与氧气、氧化铁、酸、碱反应方程式的书写。
技能目标:
①在观察与思考中,提高实验操作技能,发展观察能力。
②在交流讨论中,提高语言表达能力。
情感目标:
通过金属及其化合物,金属材料在生产和生活中的应用等的学习,提高学习化学的兴趣,
增强学好化学,服务社会的责任感和使命感。
(2)重点:Al 及其化合物的化学性质。
难点:Al 及其化合物的两性。
教学环节 | 教学内容 | 教师活动 | 学生活动 |
导入 | 1.铝作为一种金属具有的性 质。 2.铝作为一种金属材料相关 的的性质。 | 设置问题,引导思考 | 根据初中学过的金属的知识和生活经验讨论作答 |
观察思考 | 实验 1:铝与氧气反应 实验 2:铝与三氧化二铁反应 | 演示实验,引导学生 观察和思考。 | 观察并讨论实验现象,得出相关的化学反应,写出化学反应方程式。 |
实验探究 | 实验 1:铝与酸反应 实验 2:铝与碱反应 | 引导学生实验,与生 活实际联系,启发学 生学习铝的两性 | 学生实验,观察实验现象,回顾金属的还原性性质,学习铝的两性,写出化学反应 方程式。 |
(3)用教学流程图(教学设计思维)简要表示本节教学内容组织形式。
(4)“纸漏斗”上面加入少量氯酸钾,是为了镁加热后产生的热量促使氯酸钾分角产生氧气,使燃烧更加剧烈,短时内放出更多的热量,促进铝热反应发生。
化学反应方程式:
(5)铝密度较小,约为钢的 1/3 左右,常温下易被空气中的氧气氧化形成致密的氧化物薄膜,保护内部的金属继续与氧气反应,可制成轻便的日常用品;导电性仅次于银、钢和金,用作导线;氧化铝为原子晶体,熔点高,可作耐火材料;铝与金属氧化物反应表现出较强的还原性用于工业生产。
(6)板书设计:
铝及铝的化合物
一、【交流研讨】
铝的性质:
1.作为金属(金属的通性):固体、金属光泽、导电性、延展性
2.作为重要的金属材料:轻便(密度较小)、稳定(氧化物薄膜保护内部的金属继续与氧气反应)、导电性好、还原性(铝热反应)。
二、【观察思考】

三、铝与酸、碱的反应
下载233网校APP及时获取2019下半年教师资格证考试真题
面试报考:2019下半年教师资格证面试报名时间
教师资格证面试如何快速通关?面试情景还原,助你一举攻下“结构化面试+试讲+答辩”三大内容,实战通关!试听课程>>



