组成蛋白质的氨基酸由蛋白质水解而来,约30种,都是a -和L-构型,通式为RCH(NH2)COOH。其中10余种为人类必需的氨基酸,如赖氨酸、亮氨酸、色氨酸、组氨酸、精氨酸、谷氨酸和半胱氨酸等。有些直接用于临床,如精氨酸和亮氨酸用于肝昏迷、蛋氨酸用于肝硬化,组氨酸用于消化道溃疡等。
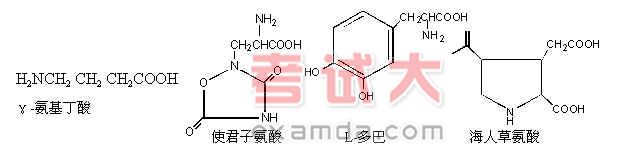
非蛋白质组成的氨基酸主要为游离状态,其中分为b 型、g 型和D-构型。其中天南星、半夏中的g -氨基丁酸(g -aminobutyric acid)具降压作用,藜豆中的L-多巴(L-dopa)用于帕金森病,使君子氨酸(squalic acid)与海人草中的a -海人草氨酸(a -kainic acid)均有驱蛔虫作用。
由于氨基酸分子中同时具有氨基和羧基,所以有两性电解质的性质。当溶pH值为该氨基酸的等电点时,其溶解度最小。借此可以用电泳法分离氨基酸。
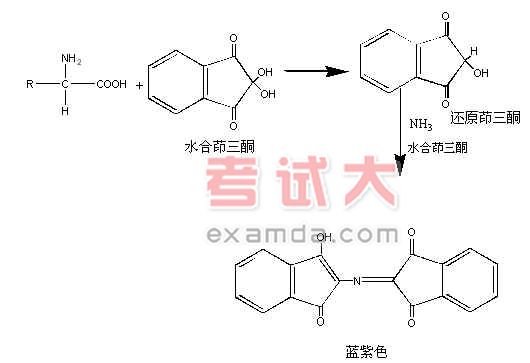
氨基酸为无色结晶。易溶于水,可溶于醇,难溶于有机溶剂。除甘氨酸外,均具旋光性,它们的旋光度决定于溶剂的性质、 pH、温度和盐的存在。许多氨基酸可与金属盐类生成络合物或分子化合物,如有些氨基酸的铜为蓝色的结晶,难溶于水,可用作提纯与精制。一般氨基酸与茚三酮 (ninhydrin)试剂反应生成蓝紫色、红紫色或紫色,而与吲哚醌(isatin)反应生成不同的颜色。此两种反应用于氨基酸的鉴别。但要注意氨气对茚三酮反应有干扰,吲哚醌反应的灵敏度不及茚三酮反应。